Pregunta 1 de 20
Exani II -> Módulos Específicos -> Química
Propiedad del carbono de combinar dos orbitales atómicos puros para formar un nuevo orbital molecular con características propias.
Isomería
Hibridación
Insaturación
Pregunta 2 de 20
Exani II -> Módulos Específicos -> Química
Identifique el compuesto relacionado con el grupo funcional éster.
Acetileno
Acetona
Propanoato de etilo
Pregunta 3 de 20
Exani II -> Módulos Específicos -> Química
Identifique el nombre IUPAC de la siguiente estructura.
2-etil-2-penteno
3-metil-3-hexeno
4-metil-3-hexeno
Pregunta 4 de 20
Exani II -> Módulos Específicos -> Química
Identifique el ejemplo que implica un proceso exotérmico.
Galvanizar un metal
Evaporar agua
Bajar la fiebre
Pregunta 5 de 20
Exani II -> Módulos Específicos -> Química
¿Cuál es el valor de la entalpía de la siguiente reacción de combustión?
CH4(g) + 2O2 → CO2(g) + 2H2O(l)
Considere los datos de entalpía parciales.
ΔHf0(O2) = 0 kJ/mol
ΔHf0(CH4(g)) = -74.81 kJ/mol
ΔHf0(H2O(l)) = -285.8 kJ/mol
ΔHf0(CO2(g)) = -393.5 kJ/mol
-890.29 kJ/mol
-604.49 kJ/mol
890.29 kJ/mol
Pregunta 6 de 20
Exani II -> Módulos Específicos -> Química
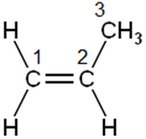
De acuerdo con la estructura, la hibridación del carbono 1 es ______, mientras que la del marcado con el número 3 es _____.
sp - sp2
sp2 - sp3
sp3 - sp
Pregunta 7 de 20
Exani II -> Módulos Específicos -> Química
¿Cuántos moles de CO2 se obtienen a partir de la combustión de 3 mol de C3H8?
Considere la siguiente ecuación: C3H8 + 5O2 → 3CO2 + 4H2O
3 mol
6 mol
9 mol
Pregunta 8 de 20
Exani II -> Módulos Específicos -> Química
Identifique el compuesto que presenta un enlace iónico.
O2
NaCl
CO
Pregunta 9 de 20
Exani II -> Módulos Específicos -> Química
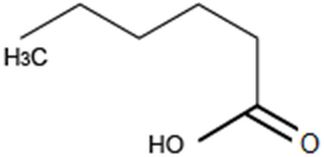
¿Cuál es el nombre del grupo funcional remarcado en el compuesto?
Cetona
Ácido carboxílico
Éter
Pregunta 10 de 20
Exani II -> Módulos Específicos -> Química
Un químico calienta en un crisol carbonato de plata a temperaturas superiores a 1 000 °C; se producen óxido de plata y dióxido de carbono.
Identifique la ecuación que representa el proceso descrito.
Ag2CO3 → Ag2O + CO2
AgCO3 → Ag2O + CO2
Ag2CO3 → AgO + CO2
Pregunta 11 de 20
Exani II -> Módulos Específicos -> Química
¿Cuál de las siguientes sustancias corresponde a una solución diluida?
Néctar de frutas
Aderezo para ensalada
Agua de sabor
Pregunta 12 de 20
Exani II -> Módulos Específicos -> Química
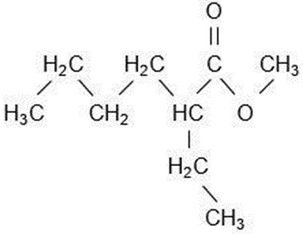
Identifique la nomenclatura IUPAC del compuesto representado en la estructura.
2-etilhexanoato de metilo
Hexanoato de 2-etil-1-metilo
Metanoato de (2-etil)pentanoilo
Pregunta 13 de 20
Exani II -> Módulos Específicos -> Química
Identifique el tipo de reacción que ocurre en la siguiente ecuación química.
H2SO4 + 2KOH → K2SO4 + 2H2O
Neutralización
Redox
Combustión
Pregunta 14 de 20
Exani II -> Módulos Específicos -> Química
Identifique los coeficientes que balancean la ecuación.
__H2SO4 + __NaHC3 → __Na2SO4 + __CO2 + __H2O
1, 1, 1, 2, 1
1, 2, 1, 2, 2
2, 1, 2, 1, 2
Pregunta 15 de 20
Exani II -> Módulos Específicos -> Química
Identifique el tipo de enlace que se forma entre los monómeros de la siguiente molécula.
Glicosídico
Glucosídico
Peptídico
Pregunta 16 de 20
Exani II -> Módulos Específicos -> Química
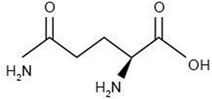
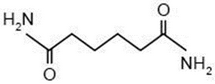
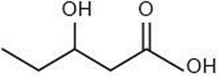
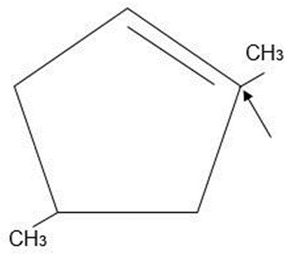
Identifique la estructura que corresponde a un aminoácido.
Pregunta 17 de 20
Exani II -> Módulos Específicos -> Química
Calcule los gramos de Al2O3 que se obtienen si se descomponen 2 mol de Al2(CO3)3 en la siguiente ecuación:
Al2(CO3)3 → Al2O3 + 3CO2
Considere:
- Al2(CO3)3 = 234 g/mol
- Al2O3 = 102 g/mol
102 g
204 g
468 g
Pregunta 18 de 20
Exani II -> Módulos Específicos -> Química
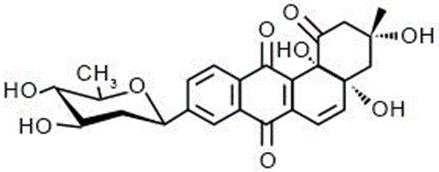
Identifique la geometría del carbono señalado en la estructura.
Trigonal plana
Tetraédrica
Lineal
Pregunta 19 de 20
Exani II -> Módulos Específicos -> Química
Se pesó 1 g de NaOH y se disolvió en 100 mL de agua. ¿Cuál es la concentración molar de la disolución resultante, considerando que la masa del NaOH es de 40 g/mol?
0.00025 M
0.25 M
0.40 M
Pregunta 20 de 20
Exani II -> Módulos Específicos -> Química
Si la diferencia de electronegatividad entre el Ca y O es de 2.5, ¿qué tipo de enlace los une para formar un compuesto?
Covalente
Iónico
Metálico

 Exani
Exani